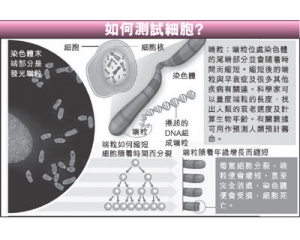
对于化学发光检测系统和多数抗体制剂来说,检测最低值可达到约2 fmol/L(10-15)的水平。相当于0.1ng 的50 000kD的蛋白质,高于此浓度的样品较易检出。一个标准的SDS –聚丙烯酰胺凝胶泳道的上样量为150µg(小胶道可为15µg),如果上样量过大条带会发生扭曲变形。因此,50kD中等大小蛋白抗原的上样量以0.1ng/150µg(或1/15 000 000)为宜。如分析的是哺乳类细胞的蛋白,这一检测最低值就相当于每个细胞有1000个50kD的蛋白分子;若要检测更低水平的蛋白,需要对抗原进行部分纯化。可采用细胞分步分离,层析或免疫沉淀的方法进行;如果待测抗原的分子量与细胞中含量丰富的蛋白(例如肌动蛋白)相近似,转膜将不会受到限制。有若干种方法常用于提高免疫印迹的灵敏度。一种是在电泳之前应用免疫沉淀法将抗原进行纯化和浓缩。该法可浓缩浓度极低浓度的抗原,并可在电泳和免疫印迹之前将其与无关的蛋白质分离,使对极低浓度抗原的研究成为可能。其它提高检测灵敏度的方法都是针对增强信号本身强度设计的。其中包括使用信号更好和更强的荧光试剂或使条带局部酶的活性增强。一些公司不断地推出新的性能更好的化学发光检测系统,而使用者则继续注重于研制更好和更灵敏的试剂。
实验室前沿,了解实验室动态
信号可通过使用三重检测系统而得到加强,例如,使一抗,二抗和三抗相继与抗原结合形成复合物。这必然使得结合物中标记抗体分子的数量增多。例如,假如有5个二抗分子可结合在一抗上,又有5个三抗分子可结合在二抗上,那么该系统就比仅用标记一抗所产生的信号增强25倍。